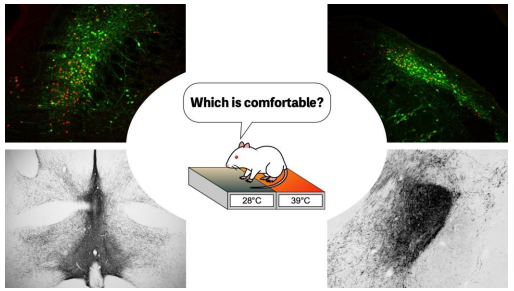
東海国立大学機構 名古屋大学大学院医学系研究科 統合生理学分野の八尋貴樹(やひろ たかき)大学院生、片岡直也(かたおか なおや)特任講師、中村和弘(なかむら かずひろ)教授の研究グループは、暑さ・寒さから逃げて快適な温度環境を探す体温調節行動を起こす脳の神経路を明らかにしました。
人間などの動物は、生命活動を行う上で適切な体温を保つため、体温調節行動を行います。カメの甲羅干しや、人間が夏に薄着をして冷房を使い、冬に厚着をして暖房を使うのも体温調節行動です。普段当たり前に行う体温調節行動ですが、この行動を起こす脳の神経メカニズムは謎でした。2017 年に研究グループは、体温調節行動を起こすために外側腕傍核(がいそくわんぼうかく)*1という脳の領域が必要であることを報告しました。今回、同グループは、外側腕傍核を介した神経伝達がどのようにして体温調節行動を起こすのかを、ラットを用いて解析しました。
その結果、皮膚の温度センサーで感知した温度感覚の情報を、外側腕傍核の異なる2つの神経細胞群が前脳の異なる領域へ伝達し、それぞれ、暑さから逃げる行動と寒さから逃げる行動を起こすことがわかりました。体温調節行動は暑さや寒さによる不快感(不快情動)によって駆動されると考えられ、今回発見した神経伝達路は、温度感覚による不快情動の形成に関わる可能性が考えられます。本研究で得られた知見は、暑さ・寒さに対して適切に不快情動を形成することができず、熱中症や低体温症に陥ってしまう原因を解明する糸口となるものです。
また、外側腕傍核のこれら 2 つの神経細胞群はともに、寒冷刺激に応じて褐色脂肪組織*2で熱を産生する反応にも必要であることがわかりました。この知見は、体温や代謝を適切に調節して健康を保つ脳の神経回路メカニズムの新たな理解を促すものであり、本研究の発展によって、糖尿病などを含む肥満症を超早期の未病段階で検出する技術や、脂肪代謝を促進する新たな肥満予防・治療の技術開発などにつながる可能性があります。
本研究成果は米国科学誌「Journal of Neuroscience」(2023 年6月 20 日付オンライン版)に掲載されました。
本研究は、国立研究開発法人科学技術振興機構(JST)ムーンショット型研究開発事業(目標2「2050 年までに、超早期に疾患の予測・予防をすることができる社会を実現」)、日本学術振興会科学研究費助成事業(基盤研究 A、B、C)、AMED 脳とこころの研究推進プログラム(領域横断的かつ萌芽的脳研究プロジェクト)、武田科学振興財団の支援を受けて実施されました。
ポイント
- 暑さから逃げて快適な温度環境を探す行動には、外側腕傍核から体温調節中枢である視索前野への神経伝達が必要である。
- 寒さから逃げて快適な温度環境を探す行動には、外側腕傍核から情動中枢である扁桃体への神経伝達が必要である。
- これらの伝達を担う外側腕傍核の 2 つの神経細胞群はともに、皮膚冷却に応じて褐色脂肪熱産生を起こすためにも必要である。
- これらの知見から、暑さと寒さに対する不快感を形成する脳の仕組みは異なると考えられ、熱中症や低体温症の発症メカニズムの解明につながる可能性がある。
- 得られた知見は、体温や代謝を適切に調節する脳の神経回路メカニズムの新たな理解を促すものでもあり、脂肪代謝を促進する新たな肥満予防・治療の技術開発などにつながる可能性がある。
1. 背景
体温調節は、動物が持つ最も基本的な生命機能の1つです。人間を含む恒温動物は体温を 37°C 前後に保つため、2つの様式の体温調節を行います。1つは「行動性体温調節*3」と呼ばれ、温度感覚による快・不快感に基づく本能的な体温調節行動を行うことで体温を保つ仕組みです。人間であれば、温度に合わせて衣服の着脱をしたり、エアコンを用いて環境温度を変えるなどの意識的な行動が体温調節行動に当たります。恒温動物のみならず、ヘビや昆虫などの変温動物でも寒い環境から逃げて暖かい環境を探す行動が見られ、行動性体温調節はほとんどの動物が普遍的に持つ仕組みです。もう1つは「自律性体温調節*4」と呼ばれ、暑い環境で汗をかいて熱を逃したり、寒い環境で筋肉を震わせて熱を作ったりするような無意識に起こる体温調節の仕組みです。恒温動物は、行動性体温調節と自律性体温調節を組み合わせることによって、効率的に体温を一定に保ちます。
近年では、地球温暖化による気温上昇の影響もあり、国内で年間数万人が熱中症で救急搬送されています。熱中症患者には高齢者が多く、暑さを感じてエアコンをつけるなどの体温調節行動をうまく行えないことがその原因の1つとされています。気温上昇と高齢化の進む日本において、適切な体温調節行動を起こす仕組みを見出し、熱中症の発症メカニズムを解明することは社会的急務となっています。しかし、自律性体温調節の神経回路の研究が進む一方で、行動性体温調節の神経回路は謎のままでした。
2017 年に同研究グループは、暑さ・寒さから逃げて快適な温度環境を探す行動を起こすためには、温度を意識の上で「感じる」ための感覚伝達神経路である脊髄視床皮質路(せきずいししょうひしつろ)*5ではなく、外側腕傍核という脳の領域を介して伝達される温度感覚情報が必要であることを報告しました。外側腕傍核は、脳の橋(きょう)と呼ばれる部位にある神経核で、体内のさまざまな感覚情報を前脳の幅広い領域に中継することが知られています。今回、研究グループは、皮膚のセンサーで感知した温度感覚情報を伝達して体温調節行動を起こす、外側腕傍核から前脳への神経路をラットを用いて解析しました。
2. 研究成果
まず研究グループは、アデノ随伴ウイルス*6を用いて、ラットの外側腕傍核の神経細胞に細胞膜移行型緑色蛍光タンパク質(palGFP)*7を発現させ、その神経線維である軸索*8を可視化しました。すると、外側腕傍核の神経細胞から伸びた軸索の終末は、視床下部にある体温調節中枢である視索前野(しさくぜんや)の正中視索前核(せいちゅうしさくぜんかく)*9と呼ばれる部位と、情動形成や恐怖記憶形成の中心として知られる扁桃体(へんとうたい)の中心核(ちゅうしんかく)*10 と呼ばれる部位に特に密集して分布することが分かりました。そこで本研究グループは、皮膚から脊髄を介して外側腕傍核に送られてきた温度情報が、外側腕傍核から正中視索前核と扁桃体中心核へ伝達され、その温度感覚情報をもとに体温調節行動が起こるという仮説(図1A)を立て、検証を行いました。
研究グループの以前の研究から、自律性体温調節には外側腕傍核から正中視索前核への温度感覚情報の伝達が必要なことが明らかになっています。一方で、外側腕傍核から扁桃体中心核へ温度感覚情報が伝達されるかは検討されていませんでした。そこで、軸索の終末から取り込まれ、神経伝達とは逆方向に運ばれて神経細胞体を標識する逆行性神経トレーサーであるコレラ毒素 B サブユニット*11を用いて、扁桃体中心核へ軸索を伸ばす外側腕傍核の神経細胞群を標識すると、この神経細胞群はラットが低温環境にいるときに活性化されること、また、正中視索前核へ軸索を伸ばす神経細胞群とは別のグループであることが明らかになりました。この実験結果から、外側腕傍核から正中視索前核あるいは扁桃体中心核へ伝達する 2 つの神経細胞群は体温調節において異なる機能を持つ可能性が示唆されました。
研究グループは、ラットの体温調節行動を解析するため、2 プレート温度選択試験を行いました。温度を自在に設定できる 2 枚の金属プレートを横並びに配置し、片方のプレートを 28°C(中性温)、他方を 39°C(高温)または 15°C(低温)に設定しました(図1B)。通常のラットは高温・低温のプレートよりも中性温のプレート上に長く滞在しました。これは、高温・低温を避けて快適な中性温環境を選ぶ暑熱・寒冷逃避行動という体温調節行動です。
そこで、軸索の終末から感染するアデノ随伴ウイルスと神経細胞体から感染するアデノ随伴ウイルスの 2 種類を組み合わせて脳に注入し、外側腕傍核から正中視索前核あるいは扁桃体中心核へ伝達する神経路をそれぞれ選択的に遮断する実験を行いました。まず、化学遺伝学的手法*12 を用いて、外側腕傍核から正中視索前核へ伝達する神経路を抑制したラットを作製しました(図2A)。このラットは、2プレート温度選択試験で暑熱逃避行動ができず、むしろ、高温のプレートの方にやや長く滞在するようになりました。一方、寒冷逃避行動は正常にできました(図2B、C)。次に、別のラットに光遺伝学的手法*13 を用いて、外側腕傍核から扁桃体中心核への神経伝達を抑制しました(図3A)。すると、寒冷逃避行動ができなくなりましたが、暑熱逃避行動は通常のラットと同じようにできました(図3B、C)。
また通常、皮膚を冷却すると、体温低下を防ぐための自律性体温調節反応として、褐色脂肪組織で熱の産生が起こります。しかし、興味深いことに、正中視索前核あるいは扁桃体中心核へ伝達する外側腕傍核のいずれかの神経細胞群に破傷風毒素軽鎖*14を発現させて神経伝達を抑制すると、皮膚冷却による褐色脂肪熱産生は起こらなくなりました(図4A)。さらに、それらのラットは暑熱環境では高体温状態になり、寒冷環境では体温低下が起こりました(図4B)。
これらの実験結果から、皮膚から脊髄を介して外側腕傍核に送られてくる温度感覚情報は正中視索前核と扁桃体中心核へ神経伝達され、正中視索前核への伝達は暑さを避けて快適な温度を選ぶ行動を、扁桃体中心核への伝達は寒さを避けて快適な温度を選ぶ行動を起こすことが明らかになりました(図5)。こうした体温調節行動は、温度感覚によって形成される不快感(不快情動)によって駆動されると考えられ、本研究成果は、暑さに対する不快情動と寒さに対する不快情動が異なる神経回路メカニズムで形成されることを示唆しています。また、外側腕傍核を介したどちらの神経路も、褐色脂肪熱産生などの自律性体温調節反応の発現に必要であることが明らかになりました。特に、扁桃体が体温調節に関わることはこれまで報告されておらず、本研究の実験結果は、体温・代謝調節を担う未知の神経回路メカニズムが存在する可能性を示しています。
3. 今後の展開
本研究成果は、暑熱逃避行動と寒冷逃避行動を生み出す脳の仕組みが異なることを世界で初めて示し、動物が普遍的に行う本能行動である体温調節行動の神経回路基盤の枠組みを明らかにしたものです。動物には、体温調節行動以外にも摂食行動、飲水行動、性行動、集団行動などの様々な本能行動があり、本能的な情動や欲求がそれらの行動を駆動します。しかし、本能行動を駆動する情動や欲求を脳の中で生み出すメカニズムはほとんど未解明です。本研究で見出した神経路は、情動中枢として知られる扁桃体などが関与し、温度感覚による快・不快感(快・不快情動)の発現を担うものと考えられます。そして、この神経路の動作原理は、他の本能行動を起こす情動や欲求の発現メカニズムとも共通する可能性があり、さらなる研究の進展によって、動物の行動全般を規定する神経メカニズムの基本原理の解明につながるかもしれません。
近年、気候変動の影響によって熱中症の罹患者が増加しており、暑さから逃避する行動の重要性が高まっています。熱中症予防のためには、暑さに対して適切な不快情動が発現し、適切な体温調節行動を行うことが重要です。本研究では、外側腕傍核から正中視索前核への温度感覚の神経伝達が遮断されると、高温から逃げられなくなるとともに、暑い環境でラットが高体温症になりました。人間の場合、特に高齢者では、皮膚の温度感知機能の低下により、外側腕傍核を介した暑熱不快感の形成が起こりにくくなるため、体温調節行動が阻害され、熱中症に陥りやすくなる可能性があります。毎年数万人に及ぶ熱中症患者を減らすためには、主観的な感覚や情動に基づく本能的な体温調節行動ではなく、客観的な気温や湿度の情報に基づく予防的な体温調節行動を促すことが必要であると考えられます。今後、この研究が進み、環境温度に対する快・不快情動発現に関わる正中視索前核や扁桃体中心核などの脳領域の活動を測定することができるようになれば、高齢者の熱中症・低体温症のリスク評価、環境温度による心身負荷の少ない衣服や室温管理システムの開発などに貢献できると考えられます。
また、本研究で同定した、正中視索前核あるいは扁桃体中心核へ伝達する外側腕傍核の 2 つの神経細胞群はともに、寒冷刺激に応じた褐色脂肪組織の熱産生を起こすためにも必要であることがわかりました。この発見は、体温や代謝を適切に調節して健康を保つ脳の神経回路メカニズムの新たな理解を促すものであり、この知見をもとに、糖尿病などを含む肥満症を超早期の未病段階で検出する技術や、脂肪代謝を促進する新たな肥満予防・治療の技術開発などにつながる可能性があります。
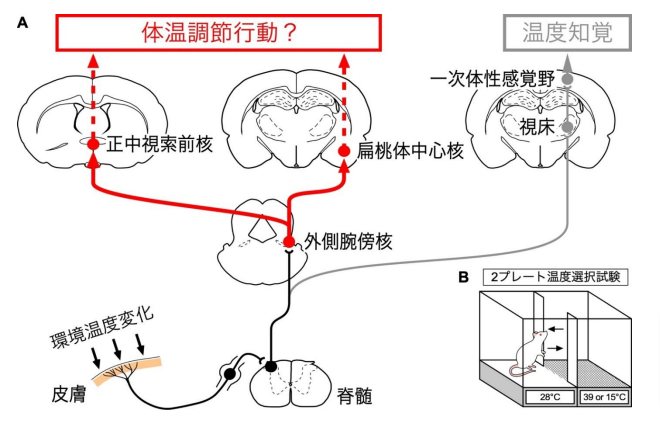
図1 本研究で検証した作業仮説
(A) 皮膚の温度受容器で感知した環境温度の感覚情報が、脊髄、外側腕傍核を経て、正中視索前核と扁桃体中心核へ伝達され、その情報をもとに体温調節行動が発現するという仮説。脊髄から視床を経て一次体性感覚野へ至る神経路(脊髄視床皮質路)が体温調節行動の発現に必要ないことは、本研究グループの以前の研究で明らかになっている。
(B) 2 プレート温度選択試験。通常のラットは、暑熱あるいは寒冷から逃避する行動を示すため、39°C または 15°C のプレートよりも、28°C のプレート上の滞在時間が長くなる。
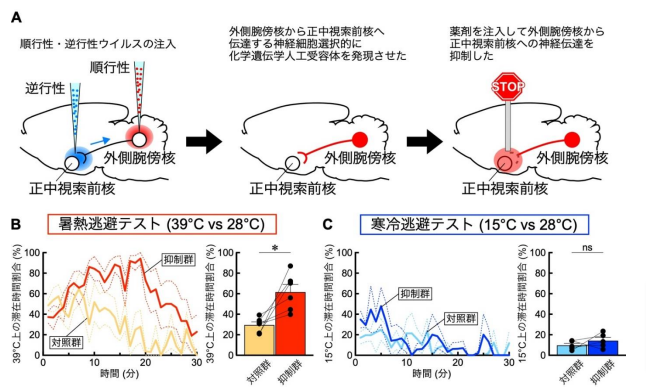
図2 暑熱逃避行動には外側腕傍核から正中視索前核への神経伝達が必要である
(A) 順行性感染するアデノ随伴ウイルスと逆行性感染するアデノ随伴ウイルスを用いた二重感染法によって、神経活動を抑制する化学遺伝学人工受容体 hM4Dinrxn を、外側腕傍核から正中視索前核へ伝達する神経細胞に選択的に発現させた。このラットの正中視索前核に hM4Dinrxn を活性化する薬物(C21)を投与することで、外側腕傍核から正中視索前核へ伸びた軸索終末の神経伝達を抑制した。
(B) 暑熱逃避テストの結果、外側腕傍核から正中視索前核への神経伝達を抑制されたラット(抑制群)は対照群と比較して 39°C のプレート上の滞在時間が有意に長かった(*P < 0.05, paired ttest)。
(C) 寒冷逃避テストでは、対照群と抑制群の間で 15°C のプレート上での滞在時間に差はなかった(ns: 有意差なし, paired t-test)。
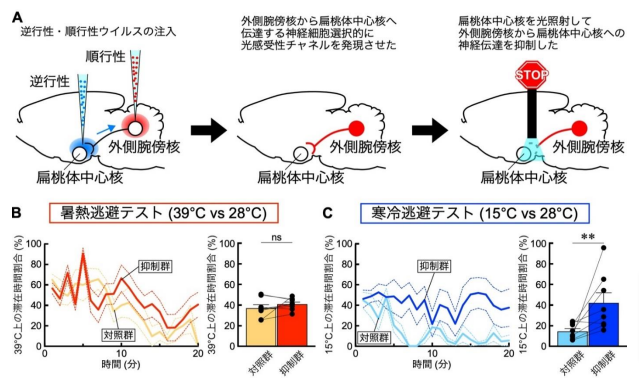
図3 寒冷逃避行動には外側腕傍核から扁桃体中心核への神経伝達が必要である
(A) 順行性感染するアデノ随伴ウイルスと逆行性感染するアデノ随伴ウイルスを用いた二重感染法によって、光感受性のイオンチャネル iChloC を外側腕傍核から扁桃体中心核へ伝達する神経細胞に選択的に発現させた。このラットの脳内に光ファイバーを挿入し、扁桃体中心核を光照射することで、外側腕傍核から扁桃体中心核へ伸びた軸索終末の神経伝達を抑制した。
(B) 暑熱逃避テストの結果、外側腕傍核から扁桃体中心核への神経伝達を抑制されたラット(抑制群)は、対照群と同程度に 39°C のプレートから逃避することができた(ns: 有意差なし, pairedt-test)。
(C) 寒冷逃避テストでは、外側腕傍核から扁桃体中心核への神経伝達を抑制されたラット(抑制群)は、対照群と比較して、15°C のプレート上での滞在時間が有意に長かった(**P < 0.01, pairedt-test)。
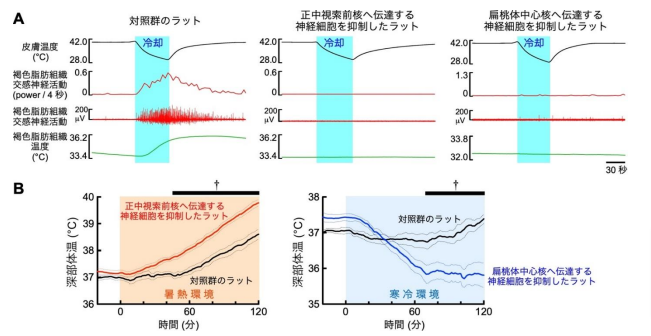
図4 正中視索前核あるいは扁桃体中心核へ伝達する外側腕傍核の2つの神経細胞群は自律性体温調節にも重要な機能を持つ
(A) ラットの体幹部の皮膚を冷却することによって、通常のラット(対照群)では褐色脂肪組織の交感神経活動と温度が上昇し、熱産生が惹起された。一方、順行性感染もしくは逆行性感染する2種類のアデノ随伴ウイルスを用いた二重感染法によって、外側腕傍核から正中視索前核あるいは扁桃体中心核へ伝達する2つの神経細胞群のそれぞれに破傷風毒素軽鎖を選択的に発現させ、神経伝達機能を抑制したラットでは、いずれも皮膚冷却による褐色脂肪熱産生は起こらなかった。
(B) 外側腕傍核から正中視索前核あるいは扁桃体中心核に伝達する2つの神経細胞群のそれぞれを破傷風毒素軽鎖で機能抑制したラットはいずれも、暑熱環境(気温 36°C)では高体温状態に陥り、寒冷環境( 気 温 4°C ) で は 体 温 低 下 が 起 こ っ た ( †P < 0.05, two-way ANOVA 後 にBonferroni’s test)。
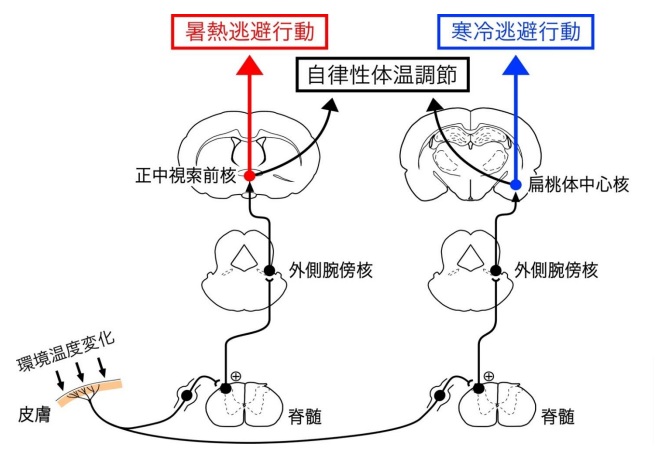
図5 本研究によって明らかになった体温調節行動を起こす2つの神経路
皮膚の温度センサーで感知した温覚(暑熱)の情報は、脊髄と外側腕傍核を経て正中視索前核へ、冷覚(寒冷)の情報は脊髄と外側腕傍核を経て正中視索前核と扁桃体中心核の両方に伝達される。外側腕傍核から正中視索前核へ伝達される温度感覚情報は暑熱逃避行動を、外側腕傍核から扁桃体中心核へ伝達される温度感覚情報は寒冷逃避行動を起こすことが明らかとなった。それぞれの経路は、暑熱あるいは寒冷の温度感覚に対する不快情動を形成し、快適な温度環境を求める体温調節行動を起こすと考えられる。また、外側腕傍核から正中視索前核と扁桃体中心核へ伝達する神経細胞群はともに褐色脂肪熱産生などの自律性体温調節反応を起こすためにも必要であることがわかった。
4. 用語説明
*1 外側腕傍核(lateral parabrachial nucleus)
脳の中脳と延髄の間に位置する、橋(きょう)と呼ばれる領域に存在する神経核。皮膚から脊髄を介して届く温度や痛みなどの感覚情報を前脳へと中継する神経核として知られる。皮膚からの情報以外に、心臓、肺、消化管などの内臓からの情報も外側腕傍核に入力され、血圧、呼吸、睡眠、摂食など様々な生体機能の調節に関わることが知られる。2017 年の本研究グループの研究で、外側腕傍核が体温調節行動に必須であることが明らかになった。
*2 褐色脂肪組織
脂肪細胞は褐色脂肪細胞と白色脂肪細胞に大別される。白色脂肪細胞は脂肪を蓄える役割を持つのに対し、褐色脂肪細胞は脂肪を蓄えるだけでなく、分解して、そのエネルギーを熱に変える役割を持つ。寒冷環境で体温低下を防ぐだけでなく、体内の余剰の脂肪を燃焼させ、肥満を防ぐ機能がある。褐色脂肪組織の熱産生は交感神経による調節を受けており、交感神経から放出されたノルアドレナリンが褐色脂肪細胞に作用すると、褐色脂肪細胞内のミトコンドリアで熱が作られる。
*3 行動性体温調節
体温調節の様式のひとつ。体温を一定域に保とうとする随意的な(自らの意志に基づく)行動、つまり体温調節行動による体温調節を指す。体温調節行動は、昆虫や魚類のような変温動物から人間を含めた恒温動物に至るまで、ほとんどの動物で観察される本能行動である。この行動は、暑いので水浴びをする、寒いので上着を羽織る、エアコンを使って部屋の温度を調節するなど多種多様な形で現れる。行動性体温調節の基盤には、環境温度を感じることで生じる心地良さや不快感(快・不快情動)を形成する脳の仕組みがあると考えられているが、その神経回路メカニズムは分かっていない。
*4 自律性体温調節
個体の意志とは無関係(不随意)に動作する自律的な仕組みによって行われる体温調節の様式。変温動物は主に行動によって体温を調節するが、恒温動物の体温維持には行動性体温調節に加えて自律性体温調節が重要な役割を担う。自律性体温調節反応には、発汗による熱の放散、皮膚血管の拡張・収縮による熱放散の調節、骨格筋のふるえによる熱の産生、褐色脂肪組織における代謝熱産生などがある。自律性体温調節反応の多くは、脳の視索前野にある体温調節中枢からの神経指令によって起こる。
*5 脊髄視床皮質路
温度を意識の上で「感じる」ために必要とされる、教科書的に知られた神経路。皮膚の温度センサーで感知した温度感覚の情報が、感覚神経を介して脊髄の後角、視床へと伝達され、さらに視床は情報を大脳皮質の一次体性感覚野へ伝達する。大脳皮質が感覚情報を処理し、意識の上で温度を「感じる」という経験につながる。
*6 アデノ随伴ウイルス(adeno-associated virus)
外部から標的の神経細胞に目的の遺伝子を導入し、発現させるために用いたウイルス。アデノ随伴ウイルスは病原性がないため安全性が高く、遺伝子治療にも利用されることがある。本研究では、神経細胞体から感染する順行性タイプと、神経の軸索(*8参照)の終末から感染する逆行性タイプの2種類を使用し、二重感染した神経細胞でのみ導入遺伝子が発現する仕組みによって、特定の脳領域間を伝達する神経細胞群の活動を人為的に抑制した。
*7 細胞膜移行型緑色蛍光タンパク質(palGFP)
青色光(波長 488 nm 周辺)を吸収して緑色蛍光(波長 510 nm 周辺)を発する緑色蛍光タンパク質(GFP)に細胞膜移行シグナル配列を付加したタンパク質。通常、GFP は細胞質中に存在するが、palGFP は細胞膜移行シグナルの働きによって細胞膜に集積するため、細胞の輪郭を神経線維の先端まで、明瞭に標識することができる。
*8 軸索(神経線維)
神経細胞体から1本伸びる細長い突起構造。活動電位(神経の電気信号)を伝導することに特化した神経線維であり、人間の場合、長いものでは 1 メートルにもおよぶ(神経細胞体の大きさは数十マイクロメートル程度)。軸索は脳内を通過しながら枝分かれし、終末で他の神経細胞と形成したシナプスを介して情報を伝達する。
*9 正中視索前核(median preoptic nucleus)
体温調節の司令塔として知られる、脳の視床下部の視索前野に存在する神経核。本研究グループは以前に、外側腕傍核の外側部と背側部の神経細胞群が、それぞれ冷覚と温覚を正中視索前核へ伝達し、自律性体温調節反応を惹起することを明らかにした。しかし、正中視索前核を含む視索前野が体温調節行動に関与するかは、長年議論が別れていた。
*10 扁桃体中心核(central amygdaloid nucleus)
情動形成や恐怖記憶形成で中心的な役割を果たす扁桃体の中の主要な神経核の1つ。扁桃体中心核はこれまで、痛み刺激に対する逃避行動や記憶形成に重要であることが報告されていたが、行動性体温調節や自律性体温調節への関与については研究されていなかった。
*11 コレラ毒素 B サブユニット(cholera toxin B-subunit)
逆行性神経トレーサーとして利用されるタンパク質の1種で、毒性は持たない。神経細胞の表面にあるGM1 ガングリオシドに結合して細胞内に取り込まれた後、軸索を通じて神経細胞体へ運ばれる。本研究では、コレラ毒素 B サブユニットを扁桃体中心核に注入することで、扁桃体中心核に軸索を伸ばす神経細胞体を標識した。
*12 化学遺伝学的手法
特定の神経細胞群の活動を操作する実験手法の一つ。 DREADD ( Designer Receptors Exclusively Activated by Designer Drug)と呼ばれる、アセチルコリン受容体を遺伝子改変した人工受容体(デザイナー受容体)を特定の神経細胞群に発現させ、この人工受容体だけを活性化できる薬物(本研究では C21 を用いた)を投与することで、この人工受容体を発現させた神経細胞群だけを活性化あるいは抑制することができる。本研究で用いた hM4Dinrxn は神経細胞を抑制する人工受容体である。hM4Dinrxnには神経終末へ運ばれるシグナル配列が付加されているため、神経終末が分布する局所に C21 を微量注入することにより、hM4Dinrxn を持つ神経終末からの神経伝達物質の放出を選択的に抑制することができる。
*13 光遺伝学的手法
特定の神経細胞群の活動を操作する実験手法の一つ。標的となる神経細胞に、特定の波長域の光に反応して開くイオンチャネルを発現させ、光を使って神経細胞の活動を人為的に操作する手法。本研究では iChloC と呼ばれる光感受性塩素イオンチャネル(抑制性オプシン)を、外側腕傍核から扁桃体中心核へ伝達する神経細胞群に発現させた後、脳内に挿入した光ファイバーを通じて扁桃体中心核の軸索終末に青色光を照射し、軸索終末における神経伝達を抑制した。
*14 破傷風毒素軽鎖
軸索終末からの神経伝達物質の放出を阻害する毒素の1種で、自然界では破傷風菌から産生される。破傷風毒素軽鎖は神経細胞内に侵入すると、軸索終末から神経伝達物質を放出する機構を構成する特定のタンパク質(SNARE タンパク質)を分解する。これにより神経伝達物質の放出が阻害され、神経伝達が遮断される。本研究では、アデノ随伴ウイルスを用いて破傷風毒素軽鎖の遺伝子を正中視索前核あるいは扁桃体中心核へ伝達する外側腕傍核の神経細胞群に導入して発現させ、それらの軸索終末からの神経伝達物質の放出を阻害した。
5. 発表論文
掲雑誌名:
Journal of Neuroscience
論文タイトル:
Two Ascending Thermosensory Pathways from the Lateral Parabrachial Nucleus That Mediate Behavioral and Autonomous Thermoregulation
著者・所属:
Takaki Yahiro1, Naoya Kataoka1,2, Kazuhiro Nakamura1
1 Department of Integrative Physiology, Nagoya University Graduate School of Medicine(名古屋大学大学院医学系研究科・統合生理学)
2 Nagoya University Institute for Advanced Research(名古屋大学・高等研究院)
DOI:
10.1523/JNEUROSCI.0643-23.2023
English ver.
https://www.med.nagoya-u.ac.jp/medical_E/research/pdf/Jou_230704en.pdf


コメント